Одним из ведущих направлений деятельности АНО «ЦИККИО» является организация, координация и поддержка кооперированных наблюдательных клинических исследований (неинтервенционных и интервенционных) в области прецизионной онкологии.
Клинические исследования
Изучение эффективности PARP-ингибитора у пациентов со злокачественными новообразованиями
с наличием нарушений в генах гомологичной рекомбинации (HRR)
Активные исследования
Составить базу данных молекулярно-генетических нарушений
в генах HRR при различных злокачественных новообразованиях в российской популяции
3
Поиск биомаркеров чувствительности и резистентности
к PARP ингибиторам
2
Изучение противоопухолевой активности и токсичности ингибитора PARP у пациентов с метастатическим онкологическим заболеванием, при его использовании по незарегистрированным показаниям на основании обнаруженных у пациента молекулярно-генетических нарушений в генах HRR
1
Цели и задачи исследования
Цели и задачи исследования
- Изучение противоопухолевой активности и токсичности ингибитора PARP у пациентов с метастатическим онкологическим заболеванием, при его использовании по незарегистрированным показаниям на основании обнаруженных у пациента молекулярно-генетических нарушений в генах HRR
- Поиск биомаркеров чувствительности и резистентности к PARP ингибиторам
- Составить базу данных молекулярно-генетических нарушений в генах HRR при различных злокачественных новообразованиях в российской популяции

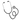
Другие солидные опухоли
Рак молочной железы
Рак яичников
Кастрационно-резистентный рак предстательной железы
Рак поджелудочной железы
Рак желудка
Уротелиальный рак
Рак эндометрия
Холангиокарцинома
Рак шейки матки
Колоректальный рак
Немелкоклеточный рак легкого
Мелкоклеточный рак легкого
Нозологии
Нозологии
- Мелкоклеточный рак легкого
- Немелкоклеточный рак легкого
- Колоректальный рак
- Рак шейки матки
- Холангиокарцинома
- Рак эндометрия
- Уротелиальный рак
- Колоректальный рак
- Рак поджелудочной железы
- Кастрационно-резистентный рак предстательной железы
- Рак яичников
- Рак молочной железы
- Другие солидные опухоли
наличие информированное согласие пациентов на участие в исследовании
наличие рекомендации междисциплинарной рабочей группы (Molecular Tumor Board) о включении в один из рукавов исследования (проводится в рамках процедуры скрининга)
наличие как минимум одного биомаркера, предсказывающего потенциальную эффективность препарата (PARP ингибитора)
После завершения молекулярного тестирования пациент будет включен для прохождения дальнейшего скрининга в одном из центов при соответствии следующим критериям:
в скрининг
Наличие биообразца опухолевой ткани (из первичной опухоли или метастатического очага) для проведения молекулярного тестирования, методом высокопроизводительного секвенирования NGS (NGS). Если тестирование уже было выполнено ранее в другой специализированной лаборатории, то необходимо предоставить соответствующее заключение
Наличие измеряемых очагов, оцениваемых по критериям RECIST 1.1
Удовлетворительная функция почек: креатинин ≤ 1.5 ВГН
и/или клиренс креатинина > 50 мл/мин)
Удовлетворительная функция печени: общий билирубин <2 х ВГН); АЛТ/АСТ < 2.5 х ВГН или не более чем в 5 х ВГН у пациентов с метастатическим поражением печени
Адекватная функция костного мозга: количество нейтрофилов>1500 х106/л, тромбоцитов >75 х 106/л, гемоглобин >90 г/л
Функциональный статус по ECOG (по классификации Восточной объединённой онкологической группы) от 0 до 2
(в течение 3 дней до начала исследуемого вмешательства)
Наличие гистологической верификации диагноза
Возраст больного старше 18 лет
Местно-распространенное (неоперабельное)
или метастатическое онкологическое заболевание
(только солидные опухоли), резистентное к стандартным видам терапии
в прескрининг
Критерии включения
- Местно-распространенное (неоперабельное) или метастатическое онкологическое заболевание (только солидные опухоли), резистентное к стандартным видам терапии
- Возраст больного старше 18 лет
- Наличие гистологической верификации диагноза
- Функциональный статус по ECOG (по классификации Восточной объединённой онкологической группы) от 0 до 2 (в течение 3 дней до начала исследуемого вмешательства)
- Адекватная функция костного мозга: количество нейтрофилов>1500×106/л, тромбоцитов >75×106/л, гемоглобин >90 г/л
- Удовлетворительная функция печени: общий билирубин <2 х ВГН); АЛТ/АСТ < 2.5 х ВГН или не более чем в 5 х ВГН у пациентов с метастатическим поражением печени
- Удовлетворительная функция почек: креатинин ≤ 1.5 ВГН и/или клиренс креатинина > 50 мл/мин)
- Наличие измеряемых очагов, оцениваемых по критериям RECIST 1.1
- Наличие биообразца опухолевой ткани (из первичной опухоли или метастатического очага) для проведения молекулярного тестирования, методом высокопроизводительного секвенирования NGS (NGS). Если тестирование уже было выполнено ранее в другой специализированной лаборатории, то необходимо предоставить соответствующее заключение
в скрининг
После завершения молекулярного тестирования пациент будет включен для прохождения дальнейшего скрининга в одном из центов при соответствии следующим критериям:
- наличие как минимум одного биомаркера, предсказывающего потенциальную эффективность препарата (PARP ингибитора)
- наличие рекомендации междисциплинарной рабочей группы (Molecular Tumor Board) о включении в один из рукавов исследования (проводится в рамках процедуры скрининга)
- наличие информированное согласие пациентов на участие в исследовании
Центры

Уважаемые пользователи, прием биоматериала на расширенное профилирование временно приостановлен. О возобновлении проекта мы сообщим дополнительно. Приносим извинения за неудобства
ФГБУ «Центральная клиническая больница с поликлиникой» УДП РФ
Москва
Стать участником исследования
Заполните поля и мы свяжемся с вами